Исторический очерк биохимии
Исторический очерк биохимии
Исторический очерк биохимии
Контрольная работа
Павлодарский государственный университет им. С.
Торайгырова
2005
Исторический очерк биохимии.
Как
самостоятельная наука биохимия сформировалась на рубеже XIX – XX веков. До
середины XIX века биохимия существовала как раздел физиологии и называлась
физиологическая химия. Однако накопление фактического материала в области
строения биологических структур, а также идентификация простейших
метаболических процессов сыграли значительную роль в становлении биохимии как
самостоятельной науки.
Бурное
развитие органической химии в первой трети XIX века оказало огромное влияние на
формирование структурной биохимии. Точкой отсчёта можно считать 1826 год, когда
Ф. Вёллер сообщил о первом синтезе органического вещества – мочевины из аммиака
и циановой кислоты. Спустя 70 лет Э. Бухнер показал, что экстракты дрожжевых
клеток переваривают крахмал, так же эффективно, как и живые дрожжевые клетки.
Обе эти работы нанесли существенный удар по витализму – учению, согласно
которому химические вещества живой природы синтезируются только с помощью
особой жизненной силы, и дали мощный импульс дальнейшему развитию биохимии.
Так, в 50 – х годах XIX века М. Бертло удалось синтезировать целый ряд
органических соединений, свойственных живой природе. М. Шеврель заложил основы
химии липидов, а Ф. Мишер открыл нуклеиновые кислоты, положив начало изучению
этого класса веществ. Однако наибольший вклад в развитие структурной биохимии
внёс Э. Фишер своими блестящими работами по анализу аминокислот, жиров и
липидов.
Исследования
процессов метаболизма также началось на рубеже XIX века. На основе открытого
М.В. Ломоносовым закона сохранения материи и накопившихся к концу XVIII века
экспериментальных данных французского учённого А. Лавуазье количественно
исследовавший и объяснивший сущность дыхания, отметив роль кислорода в этом
процессе. Работы Лавуазье стимулировали исследования по энергетике метаболизма
и уже в начале XIX века были определены количество теплоты при сгорании 1 г.
жиров, белков и углеводов. Примерно в это же время, работали Дж. Присли и Я.
Ингенхуза был открыт процесс фотосинтеза. Из живых объектов К. Шесле выделил
ряд органических кислот, Д. Руэль – мочевину, Ф. Конради – холестерин.
В
XX веке большое число открытий привело к подлинному рассвету биохимии.
Фундаментальные исследования в области энзимологии, химии белков, липидов,
углеводов, идентификация молекулярных механизмов основных обменных процессов, а
также структур и функций генома, вывели биохимию на уровень основной
количественной биологической науки. Велика роль российских учёных в становлении
и развитии биохимии. Приоритетные исследования белков и аминокислот (А.Я.
Данилевский, С.С. Салазкин, М.В. Ненцкий и другие); витаминов (Н.И. Лунин, К.А.
Сосик, В.В. Пашутин); тканевого дыхания (А.Н.Бах, В.И. Палладин);
трансаминирования аминокислот (А.Е. Браунштейн) ; механизмов механохимического
сопряжения (В.А. Энгельчардт) ; химии нуклеиновых кислот и механизмов
биосинтеза белка (А.Н. Белозёрский, А.С. Спирин) ; биоэнергетике (В.П.
Скулачёв); структуры и функции генома (Г.П. Георгиев) и работы других
российских учёных внесли огромный вклад в современную биохимию.
Биологическая
биохимия изучает различные структуры, свойственных живым организмам, и
химические реакции, протекающие на клеточном и организменном уровнях. Основой
жизни является совокупность химических реакций, обеспечивающих обмен веществ.
Таким образом, биохимию можно считать основным языком всех биологических наук.
В настоящее время как биологические структуры, так и обменные процессы,
благодаря применению эффективных методов, изучены достаточно хорошо. Многие
разделы биохимии в последние годы развивались столь интенсивно, что выросли в
самостоятельные научные направления и дисциплины. Прежде всего можно отметить
биотехнологию, генную инженерию, биохимическую генетику, экологическую
биохимию, квантовую и космическую биохимию и так далее. Велика роль биохимии в
понимании сути патологических процессов и молекулярных механизмов действия
лекарственных веществ.
Общая характеристика витамина А. Биохимические
функции. Авитаминоз.
Витамин
А был открыт Н. Друшмандом в 1916 году. Этому открытию предшествовали
наблюдения о наличии жирорастворимого фактора в пище, необходимого для
нормального развития сельскохозяйственных животных. В дальнейшем было
установлено, что имеется три витамина группы А: ретинол, или витамин А1,
неоретинол – стереоизомер А1 и А2. Этот витамин необходим не только животным,
но и человеку, и при его дефиците у человека появляются заболевания глаз –
ксерофтальмия и гемералопия. Витамин группы А содержится только в животных
продуктах, таких, как печень, рыбий жир, сливочное масло и других. В
растительной пищи содержаться поратинойды, способные предупреждать А –
авитаминоз. При поступлении в организм человека или животных они под влиянием
фермента каротиназы превращаются в витамин А1. Ретинол представляет собой
непредельный одноатомный спирт, состоящий из бета – ионного кольца, а также
боковой цепи, содержащей два остатка изопрена и первичную спиртовую группу:
Витамин А – ретинол.
Витамин
А2 отличается от ретинола наличием дополнительной двойной связью в бета –
ионном кольце. Потребность человека в витамине А составляет 1,5 мг.
Витамин
А и соответствующие провитамины – каротиноиды широко распространены в природе и
находятся в основном в животных организмах.

Витамин
А поступая в организм как в свободном, так и в эстерифицированном виде.
Свободный ретинол сорбируется слизистой кишечника, а его эфиры сначала
гидролизуются при помощи фермента гидролазы эфиров карбоновых кислот. На
внутренней поверхности ворсинок кишечника происходит ресинтез эфиров ретинола,
которые затем поступают в кровь или лимфу. В лимфе более 90 % витамина А
находится в эстерифицированном состоянии. В крови витамин А связывается со
специфическим ретинолом – связывающим белком, а затем депонируется в печени. Благодаря
этому концентрация витамина А в сыворотке крови более или менее постоянна даже
при некотором дефиците этого витамина в пище.
Витамин
А в организме осуществляет разнообразные функции. Вскоре после открытия была
установлена его необходимость для нормального роста, а также для процесса
сперматогенеза. В дальнейшем было показано, что витамин А необходим для
нормального эмбрионального развития, а его окислённая форма – ретиновая кислота
– контролирует ростовые процессы. Биохимическая основа действия витамина А чаще
всего связанна с влиянием на проницаемость клеточных мембран. С помощью
радиоизотопной технике было установлено также, что витамин А сорбируется на
мембранах эндоплазматического ретикулума, влияя на созревание и транспорт
секреторных белков. Велика роль витамина А в фотохимических процессах зрения. В
зрительном акте можно выделить изменение конформации пигментов под действием
кванта света, формирование нервного импульса, а также релаксацию пигмента в
исходное состояние. Пигмент, состоящий из ретиналя и белка опсина, называется
родопсином, при замене ретиналя на гидроретиналь образуется порфиропсин.
Пигменты локализованы в колбочках, расположенных в мембране сетчатки. При
фотохимической реакции происходит поглощение квантов световой энергии зрительным
пигментом – родопсином. Родопсин, который в качестве хромофора содержит 11 –
цис – ретиналь, под действием света превращается в нестабильный продукт
лумиродопсин. При этом происходит изменение конформации молекулы родопсина,
которые инициирует формирование нервного импульса передающегося в мозг. Затем в
результате фотоизомеризации образуется полный транс – ретиналь, который в
конечном счёте распадается на транс – ретиналь и белок опсин. В результате
действия фермента ретиналь изомеразы полный транс – ретиналь, который в темноте
взаимодействует с опсином и регенерирует родопсин.
Среди
заболеваний у людей, особенно в детском возрасте, связанных с недостатком
витамина, гипо – и авитаминоз А встречаются относительно часто. Они обусловлены
недостаточным поступлением витамина А с пищей или нарушением резорбции и обмена
этого витамина ( эндогенное происхождение ).
По
данным ВОЗ в мире ежегодно наблюдается не менее 100000 случаев ксерофтальмии.
Наиболее частой причиной слепоты в Южной и Восточной Азии является перенесённая
в детстве ксерофтальмия.
В
НРБ клиническое появление авитаминоза А – явление крайне редкое.
У
здоровых людей при смешанной диете потребности в витамине А обычно
удовлетворяются. Пища, бедная животными белками, как правило, бедна и
ретинолом. Поэтому гипо – и авитаминоз А сопровождается недостаточностью белков
и гипотрофией.
Растительная
пища, а главным образом зеленолистые овощи, как и овощи и фрукты жёлто –
оранжевого цвета, к которым относятся морковь, абрикосы, шиповник, перец,
помидоры и другие, содержат только провитамин А. Из каротиноидов витамин А –
активностью обладают только бета – каротины ( приблизительно равна 1/6
активности ретинола ). Активность выражается в международных единицах: 1 МЕ
витамин А = 0,3 мкг. Ретинола или 0,6 мкг. бета – каротина. Резорбция и
превращение β – каротина в витамин А осуществляется в клетках кишечной
мукозы, откуда по лимфатическому пути переносится и депонируется в печени.
Посредством специфического транспортного белка ретинол переносится из печени к
месту действия – клетке.
Подобно
резорбции нейтральных жиров, витамин А в кишечнике нарушается при отсутствии
панкреатической липазы и желчи, а также при нарушении функции слизистой
оболочки кишечника, целиакии, целиакоподобном синдроме, фиброзе поджелудочной железы,
циррозе печени, обтурационной желтухе, мальабсорбционном синдроме и некоторых
также острых инфекционных заболеваниях. К последним относятся: сепсис, тяжёлая
пневмония или тяжёлый гломерулонефрит, а также некоторые интоксикации с
поражением печени. В следствии увеличенной экскреции гиповитаминоз А возможен и
при хронических инфекционных заболеваниях и инфекциях мочевых путей.
При
белковом голодании снижается белок, переносящий ретинол из печени и тканям, и
уровень витамина А в плазме резко снижается.
Витамин
А устойчив при обычной варке, разрушается при высокой температуре, при сушке и
под влиянием окислителей. От окисления его предохраняет витамин Е.
В
печени имеются значительные резервы витамина А, поэтому клинические проявления
авитаминоза А наступают после продолжительного его дефицита.
Витамин
А участвует в образовании фоточувствительных пигментов в сетчатке и
обеспечивает ночное зрение, принимает участие в развитии костной ткани, в
созревании эпителия кожи и слизистых глаз, пищеварительной, дыхательной и
мочеполовой системы. Он играет важную роль в процессе ороговения и образования
слизи.
Известна
роль витамина А в стабильности мембран. Большие дозы приводят к руптурам
лизосомных мембран с освобождением гидролаз. Подобные явления наблюдаются и при
дефиците. При недостаточном поступлении витамина А клинические явления
соответствуют нарушенным функциям организма, при осуществлении которых витамин
А играет существенную роль. Понижение содержание витамина А в крови,
соответственно в сетчатке, приводят к нарушению ночного зрения (“куриная
слепота” – гемералопия) в следствии нарушения цикла зрительного пурпура.
Участие витамина А в формировании клеток особенно отчётливо проявляется по
отношению эпителия: при дефиците витамина А в эпидермисе и в эпителии слизистых
наступают атрофические изменения базальных слоёв с плоско – клеточной
метаплазией и ороговением. При дефиците витамина А в связи с отсутствием его
воздействия на хрящевые клетки прекращается эндохрондральное окостенение как
результат нарушения деления ядра и созревания хрящевых клеток в эпифизах.
О
механизме общего неблагоприятного воздействия на организм дефицита витамина А,
в смысле его влияния на рост, массу тела и устойчивость по отношению к
инфекционным возбудителям, можно судить по некоторым биохимическим и
морфологическим изменениям. Отставание роста и массы тела связывается с
нарушением белкового обмена. Это отставание проявляется ещё больше при усилении
катаболических процессов, обусловленными продолжительными вторичными инфекциями
кожи и слизистых. Нарушение окостенения в эпифизах длинных трубчатых костей
вызывает замедление роста в длину.
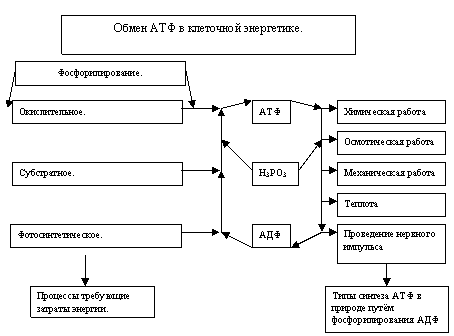
Роль АТФ.
Как
известно в биоэнергетике живых организмов имеют значение два основных момента:
а)
химическая энергия запасается путём образования АТФ, сопряжённого с
экзергоническими катаболическими реакциями окисления органических субстратов;
б)
химическая энергия утилизируется путём расщепления АТФ, сопряжённого с
эндергоническими реакциями анаболизма и другими процессами, требующими затраты
энергии.
Встаёт
вопрос, почему молекула АТФ соответствует своей центральной роли в
биоэнергетике. Для его разрешения рассмотрим структуру АТФ
Структура АТФ4 –( при рН 7,0 тетразаряд аниона).
АТФ
представляет собой термодинамически нестойкое соединение. Нестабильность АТФ
определяется, во – первых, электростатическим отталкиванием в области кластера
одноимённых отрицательных зарядов, что приводит к напряжению всей молекулы,
однако сильнее всего связи – Р – О – Р, и во – вторых, конкретным резонансом. В
соответствии с последним фактором существует конкуренция между атомами фосфора
за неподелённые подвижные электроны атома кислорода, расположенного между ними,
поскольку на каждом атоме фосфора имеется частичный положительный заряд в
следствии значительного электронаицепторного влияния групп Р=О и Р – О-. Таким
образом, возможность существования АТФ определяется наличием достаточного
количества химической энергии в молекуле, позволяющей компенсировать эти физико
– химические напряжения. В молекуле АТФ имеется две фосфоангидридных
(пирофосфатных) связи, гидролиз которых сопровождается значительным уменьшением
свободной энергии (при рН 7,0 и 37оС).
АТФ+Н2О
= АДФ + Н3РО4 ΔG0I = -31,0 КДж/моль.
АДФ+Н2О
= АМФ +Н3РО4 ΔG0I = -31,9 КДж/моль.
Одной
из центральных проблем биоэнергетики является биосинтез АТФ, который в живой
природе происходит путём Фосфорилирование АДФ.
Фосфорилирование
АДФ является эндергоническим процессом и требует источника энергии. Как
отмечалось ранее, в природе преобладает два таких источника энергии – это
солнечная энергия и химическая энергия восстановленных органических соединений.
Зелёные растения и некоторые микроорганизмы способны трансформировать энергию,
поглощённых квантов света в химическую энергию, которая расходуется на
фосфорилирование АДФ в световой стадии фотосинтеза. Этот процесс регенерации
АТФ получил название фотосинтетического фосфорилирования. Трансформация энергии
окисления органических соединений в макроэнергетические связи АТФ в аэробных
условиях происходит преимущественно путём окислительного фосфорилирования.
Свободная энергия, необходимая для образования АТФ, генерируется в дыхательной
окислительной цепи митаходрий.
Известен
ещё один тип синтеза АТФ, получивший название субстратного фосфорилирования. В
отличии от окислительного фосфорилирования, сопряжённого с переносом
электронов, донором активированной фосфорильной группой (- РО3 Н2), необходимой
для регенерации АТФ, являются интермедианты процессов гликолиза и цикла
трикарбоновых кислот. Во всех этих случаях окислительные процессы приводят к
образованию высокоэнергетических соединений: 1,3 – дифосфоглицерата (гликолиз),
сукцинил – КоА (цикл трикарбоновых кислот), которые при участии соответствующих
ферментов способны фолирировать АДФ и образовывать АТФ. Трансформация энергии
на уровне субстрата является единственным путём синтеза АТФ в анаэробных
организмах. Этот процесс синтеза АТФ позволяет поддерживать интенсивную работу
скелетных мышц в периоды кислородного голодания. Следует помнить, что он
является единственным путём синтеза АТФ в зрелых эритроцитах не имеющих
митохондрий.
Особо
важную роль в биоэнергетике клетки играет адениловый нуклеотид, и которому
присоединены два остатка фосфорной кислоты. Такой вещество называется
аденозинтрифосфорной кислотой (АТФ). В химических связях между остатками
фосфорной кислоты молекулы АТФ запасена энергия, которая освобождается при
отщеплении органического фосфорита: АТФ= АДФ+Ф+Е, где Ф – фермент, Е –
освобождающая энергия. В этой реакции образуется аденозинфосфорная кислота
(АДФ) – остаток молекулы АТФ и органический фосфат. Энергию АТФ все клетки
используют для процессов биосинтеза, движения, производство тепла, нервных
импульсов, свечений (например, улюминисцентных бактерий), то есть для всех
процессов жизнедеятельности.
АТФ
– универсальный биологический аккумулятор энергии. Световая энергия,
заключенная в потребляемой пище, запасается в молекулы АТФ.
Запас
АТФ в клетке невелик. Так, в мышце запаса АТФ хватает на 20 – 30 сокращений.
При усиленной, но кратковременной работе мышцы работают исключительно за счёт
расщепления содержащейся в них АТФ. После окончания работы человек усиленно
дышит – в этот период происходит расщепление углеводов и других веществ (
происходит накопление энергии) и запас АТФ в клетках восстанавливается.
Глюкоза. Формула глюкозы.
Сахара
имеют общую формулу С(Н2О)n, где n – целое число (от 3 до 7).
Всё
сахара содержат гидроксильные, а также либо альдегидные, либо китонные
группировки. Взаимодействую друг с другом, моносахара могут образовывать ди-,
три- или олигосахариды. Сахара являются главным энергетическим субстратом
клеток. Кроме того, они образуют связи с белками и липидами, а также являются
строительными блоками при образовании более сложных биологических структур.
Основными реакционоспособными группировками сахаров являются гидроксильные
группы, участвующие, в частности, в образовании связей между мономерами.
Во
всех клетках способных метаболизировать глюкозу, первой реакцией является её
фосфорилирование до глюкозо – 6 – фосфата. Реакция катализируется ферментом
гексокиназой, а донором фосфорильной группы является молекула АТФ.
Эта
реакция практически необратима, дельта G0I= -16,74 КДж/моль. Гексокиназа,
присутствующая во всех тканях, за исключением паренхимы печени имеет высокое
средство к глюкозе, а также способна фосфорилировать и другие гексозы, но
значительно с меньшей скоростью. В клетках печени эту функцию выполняет
глюкокиназа, активность которой зависит от питания. Глюкокиназа специфична к
глюкозе и эффективно функционирует только при высокой концентрации в крови
глюкозы. Важным свойством глюкокиназы является ингибирование продуктом реакции
глюкозо – 6 – фосфатом по аллостерическому механизму.
Фосфорилированная
глюкоза не способна проходить через цитоплазматическую мембрану и оказывается
“запертой” в клетке. Таким образом, глюкозо – 6 – фосфат является центральным
метаболитом углеводного обмена и занимает важное положение в интеграции ряда
метаболических путей (гликолиз, глюкогинез, пентозофосфатный путь,
гликогенолиз).
Обратный
процесс дефосфорилирования глюкозы идёт только в трёх тканях, клетки которых
способны транспортировать глюкозу в кровь, а именно ткани печени, эпителия
почечных канальцев тонкого кишечника. Это становится возможным благодаря
действию гидролитического фермента глюкозо – 6 – фосфатазы, который
катализирует реакцию:
О
регуляции активности этого фермента до сих пор известно мало, а следовательно,
неясно, какие факторы предотвращают непрерывный цикл фосфорилирования и
дефосфорилирования глюкозы.
В
растительном мире огромные количества глюкозы образуется путём восстановления
диоксида углерода в процессе фотосинтеза. В организме животных глюкоза
непрерывно синтезируется в строго регулируемых реакциях из простых
предшественников. Предшественниками могут быть: 1) пируват или лактат; 2)
некоторые аминокислоты; 3) любой другой компонент, который в процессе
катаболизма может превращён в пируват или один из метаболитов ЦТК.
Биосинтез
глюкозы из неуглеводных предшественников носит название глюконеогенез, а
пируват обуславливает вхождение в этот процесс. Как отмечалось выше, в процесс
глюконеогенеза вовлекают ряд аминокислот, после превращения их в пируват или
оксалоацетат. Также аминокислоты получили название глюкогенных. Из продуктов
деградации триацилглицералов только глицерол может участвовать в глюконеогенезе
путём превращения его в дегидроксиацетон ( метаболит гликолиза), а затем в
глюкозу.
Подобно
тому как гликолиз представляет собой центральный путь катаболизма глюкозы, в
процессе которого она распадается до двух молекул пирувата, превращение
последних в глюкозу составляет центральный путь глюконеогенеза. Таким образом,
глюконеогенез в основном протекает по тому же пути, что и гликолиз, но в
обратном направлении. Однако три реакции гликолиза ( глюкоза > глюкозо – 6 –
фосфат; фруктозо – 6 – фосфат > фруктозо – 1,6 – дифосфат; фосфоеноилпируват
> пируват) необратимы, и в обход этих реакций в глюконеогенезе протекают другие
реакции с иной стехиометрией, катализируемые другими ферментами. Известны 4
фермента, катализирующие реакции глюконеогенеза и не принимающие участие в
гликолизе: пируваткарбоксилаза, фосфоеноилпируваткарбоксилаза, фруктозо – 1,6 –
диофосфотаза, глюкозо – 6 – фосфотаза.
Они
локализованы преимущественно в печени, где и происходит главным образом
глюконеогенез. Значительно менее интенсивно этот процесс идёт в корковом
веществе почек.
После
того как в мышцах истощается запас глюкогена, основным источником пирувата
становится аминокислоты, образующиеся после деградации белков. При этом более
30% аминокислот, поступающих из крови в печень, приходится на аланин – одну из
глюкогенных аминокислот, углеродный скелет которой используется в печени как
предшественник для синтеза глюкозы. Другим источником пирувата является лактат,
который накапливается в интенсивно работающих мышцах в процессе анаэробного
гликолиза, когда митохондрии не успевают реокислить накапливающийся НАДН.
Лактат транспортируется в печень, где снова превращается в пируват, а затем в
глюкозу и гликоген. Этот физиологический цикл называется циклом Кори (по имени
его первооткрывателя). У цикла Кори две функции – сберечь лактат для
последующего синтеза глюкозы в печени и предотвратить развитие ацидоза.
Энергетика обмена.
Обмен
веществ (метаболизм) – это совокупность протекающих в живых организмах
химических превращений, обеспечивающих их рост, жизнедеятельность,
воспроизведение, постоянный контакт и обмен с окружающей средой. Благодаря
обмену веществ происходит расщепление и синтез молекул, входящих в состав
клеток, образование, разрушение и обновление клеточных структур и межклеточного
вещества . Например, у человека половина всех тканевых белков расщепляется и
строится заново в среднем в течении 80 суток, белки печени и сыворотки крови
наполовину обновляются каждые 10 суток, а белки мышц – 180, отдельные ферменты
печени – каждые 2 – 4 часа. Обмен веществ неотделим от процессов превращения
энергии: потенциальная энергия химических связей сложных органических молекул в
результате химических превращений переходит в другие виды энергии, используемой
на синтез новых соединений, для поддержания структуры и функции клеток,
температуры тела, для совершения работы и так далее. Все реакции обмена веществ
и превращения энергии протекают при участии биологических катализаторов –
ферментов. У самых разных организмов обмен веществ отличается упорядочностью и
сходством последовательности ферментативных превращений, несмотря на большой
ассортимент химических соединений, вовлекаемых в обмен. В тоже время для
каждого вида характерен особый, генетическизакреплённый тип обмена веществ,
обусловленный условиями его существования.
Обмен
веществ складывается из двух взаимосвязанных, одновременно протекающих в
организме процессов – ассимиляция и диссимиляция, или анаболизм и катаболизм. В
ходе катаболических превращений происходит расщепление крупных органических
молекул до простых соединений с одновременным выделением энергии, которая
запасается в форме богатых энергией фосфатных связей, главным образом в
молекуле АТФ и других богатых энергией соединений. Катаболические превращения
обычно осуществляются в результате гидролитических и окислительных реакций и
протекает как в отсутствии кислорода (анаэробный путь – гликолиз, брожение),
так и при его участии (аэробный путь – дыхание). Второй путь эволюционно более
молодой и в энергетическом отношении более выгодный. Он обеспечивает полное
расщепление органических молекул до СО2 и Н2О. Разнообразные органические
соединения в ходе катаболических процессов превращаются в органическое число
небольших молекул (помимо СО2 и Н2О): углеводы – в трифосфаты и (или) пируват,
жиры – в ацетил – КоА, пропионил – КоА, оксалоацетат, α – кетоглютарат,
фумарат, сукцинат и конечные продукты азотистого обмена – мочевину, аммиак,
мочевую кислоту и другие.
В
ходе анаболических превращений происходит биосинтез сложных молекул из простых
молекул – предшественников. Автотрофные организмы (зелёные растения и некоторые
бактерии) могут осуществлять первичный синтез органических соединений из СО2 с
использованием энергии солнечного света (фотосинтез) или энергии окисления
неорганических веществ. Гетеротрофы синтезируют органические соединения только
за счёт энергии и продуктов, образующихся в результате катаболических
превращений. Исходным сырьём для процессов биосинтеза в этом случае служит
небольшое число соединений, в том числе ацетил – КоА, сукцинил КоА, рибоза,
пировиноградная кислота, глицерин, глицин, аспарагиновая, глутаминовая и другие
аминокислоты. Каждая клетка синтезирует характерные для неё белки, жиры,
углеводы и другие соединения. Например, глюкоген мышц синтезируется в мышечных
клетках, а не доставляется кровью из печени. Как правило, синтез включает
восстановительные этапы и сопровождается потреблением энергии.
Функции липидов.
Липиды
(от греческого “липос” – жир) – низкомолекулярные органические соединения
полностью или почти полностью нерастворимые в воде, могут быть извлечены из
клеток животных, растений, и микроорганизмов неполярными органическими растворителями,
такими как хлороформ, эфир, бензол.
Гидрофобность
(или липофильность) является отличительным свойством этого класса соединения,
хотя по природе химическому строению и структуре – они весьма разнообразны. В
их состав входят спирты, жирные кислоты, азотистые соединения, фосфорная
кислота, углеводы и другие. Следовательно, учитывая различия в химическом
строении, функциях соединений, относящихся к липидам, дать единое определение
для представителей этого класса веществ невозможно.
Роль
липидов в процессе жизнедеятельности организма велика и разнообразна. К
основным функциям липидов относятся структурная, энергетическая, резервная,
защитная, регуляторная.
Структурная функция.
В
комплексе с белками липиды являются структурными компонентами всех биологических
мембран клеток, а следовательно, влияют на их проницаемость, участвуют в
передаче нервного импульса, в создании межклеточного взаимодействия и других
функциях биомембран.
Энергетическая функция.
Липиды
являются наиболее энергоёмким “клеточным топливом”. При окислении 1г. жира
выделяется 39 КДж энергии, что в два раза больше, чем при окислении 1г.
углеводов.
Резервная
функция.
Липиды
являются наиболее компактной формой депонирования энергии в клетке. Они
резервируются в адипоцитах – клетках жировой ткани. Содержание жира в организме
взрослого человека составляет 6 – 10 кг.
Защитная
функция.
Обладая
выраженными термоизоляционными свойствами, липиды предохраняют организм от
термических воздействий; жировая прокладка защищает тело и органы животных от
механических и физических повреждений; защитные оболочки в растениях (восковой
налёт на листьях и плодах) защищает от инфекции и излишней потери или
накопления воды.
Регуляторная
функция.
Некоторые
липиды являются предшественниками витаминов, гормонов, в том числе гормонов
местного действия – эйкозаноидов: простагландинов, тромбоксанов и лейкотриенов.
Регуляторная функция липидов проявляется также в том, что от состава свойств,
состояния мембранных липидов во многом зависит активность мембранно – связанных
ферментов.
У
бактерий липиды определяют таксономическую индивидуальность, дифференциацию
видов, тип патогенеза и многие другие особенности. Нарушение липидного обмена у
человека приводит к развитию таких патологических состояний, как атеросклероз,
ожирение, метаболический ацидоз, желчнокаменная болезнь и других.
Список литературы
1
В.П. Комов., В.Н. Шведова “Биохимия” – М.:”Дрофа” 2004 г.
2
Гл. ред. М.С. Гиляров. Ред.кол.: А.А. Абаев, Г.Г. Винберг, Г.А. Гаварзин и др.
“Биологический энциклопидический словарь” – М.: Современная энциклопедия 1986
г.
3
З.А. Власова “Биология. Пособие для поступающих в ВУЗ” – М.: Филологическое
общество Слово “Эксмо” 2003 г.
4
Под ред. Пр. Бр.Батанова “Клиническая педиатрия”: София 1988г.
Для
подготовки данной работы были использованы материалы с сайта http://ref.com.ua
|



